2.05.2022 р.
Тема: Електричний струм у розчинах та розплавах електролітів. Застосування електролізу
Теорія:
Що таке електричний струм в рідинах?
У посудину з дистильованою водою опустимо два електроди. Зберемо коло із джерела струму, ключа, лампочки та чутливого амперметра. Якщо замкнути коло, то стрілка амперметра не відхилиться. Це означає, що дистильована вода не містить вільних носіїв заряду й у колі немає струму.
У такий же спосіб можна переконатися, що суха кам’яна сіль так само є діелектриком.
А тепер «об’єднаємо» ці два діелектрики: насиплемо у посудину з водою дві-три ложки кам’яної солі. Ми побачимо, що лампочка загориться, причому в міру розчинення солі розжарення лампи збільшується.
Цей дослід доводить, що підсолена вода є провідником, причому носії заряду з’являються під час розчинення солі у воді.
За допомогою подібних дослідів можна визначити, що практично усі водні розчини солей, кислот і лугів є провідниками електричного струму.
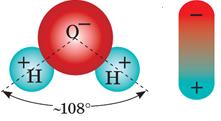
Наприклад, у молекулах кухонної солі NaCl позитивно заряджений йон натрію
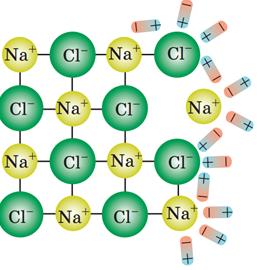
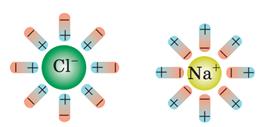
Таким чином, носіями заряду в електролітах є йони, тобто електроліти мають йонну провідність.
У розчині може відбуватися також процес, що називається рекомбінацією.
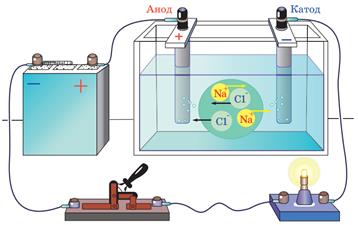
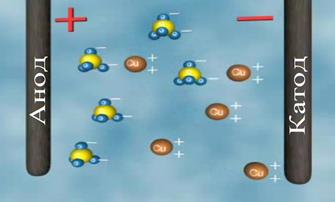
Опустимо електроди в посудину з електролітом, наприклад, із водним розчином кухонної солі
позитивні йони рухаються до негативного електрода — катода, тому їх називають катіонами;
негативні йони рухаються до позитивного електрода — анода, і їх відповідно називають аніонами.
Зазначимо, що зі збільшенням температури кількість йонів у електроліті збільшується, відповідно збільшується й сила струму.
При нагріванні електроліту сила струму збільшується, отже опір зменшується.
Якщо струм проходить крізь розчин мідного купоросу, то із часом виявимо, що на катоді утворився тонкий шар міді.
m — маса речовини;
k — електрохімічний еквівалент;
q — електричний заряд.
Очищають метали (рафінування) (мідь, срібло тощо).
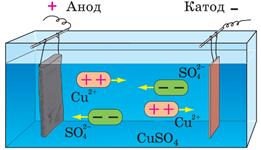
Рафінування міді: тонка пластинка чистої міді є катодом, товста пластинка неочищеної міді — анодом; ванна наповнена водним розчином купрум
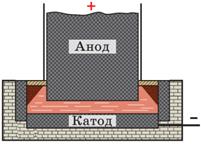
Розглянемо схему промислового пристрою виробництва алюмінію. Дно та стінки ванни слугують катодом; алюміній збирається на дні ванни. Вугільний блок слугує анодом, на ньому виділяється кисень.
За допомогою електролізу можна наносити тонкий шар металу на поверхню виробу — робити сріблення, золочення, нікелювання, хромування тощо. Такий шар може захищати від корозії, збільшувати міцність виробу або просто ставати його прикрасою.
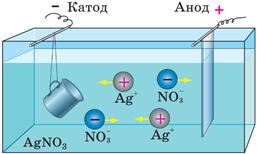
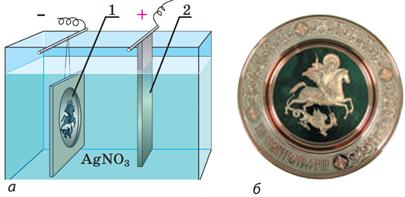
а — схема пристрою: восковий зліпок, покритий тонким шаром графіту, є катодом
б — одержана копія
Приклад розв’язування задач.
Унаслідок електролізу розчину хлоридної (соляної) кислоти НС1 на катоді за деякий час виділилося 75 г водню. Скільки хлору виділилося за цей самий час на аноді? Електрохімічні еквіваленти водню й хлору відповідно дорівнюють 0,0104 мг/Кл і 0,367 мг/Кл.

Розв'язання
mH2 = КH2 ∙ q
mCl2 = КCl ∙ q


Відповідь: на аноді виділиться 2,65 кг хлору.
Підсумки
• Водні розчини солей, кислот і основ, а також їх розплави називають електролітами.
• Носіями електричного струму в електролітах є йони обох знаків — позитивно заряджені (катіони) і негативно заряджені (аніони).
• Електроліз — виділення речовини на електродах під час проходження електричного струму через електроліт.
• Закон електролізу (закон Фарадея): маса виділеної на електроді речовини прямо пропорційна заряду, що пройшов через електроліт: m = k ∙ q, де k — електрохімічний еквівалент речовини: m = k ∙ I ∙ t.
• Електроліз широко застосовують у техніці.
Коментарі
Дописати коментар